- Son Dakika
- Gündem
- Ekonomi
- Finans Ekstra+
- Yazarlar
- Sektörel
- Dünya
- Kültür-Sanat
- Teknoloji
- FOTOĞRAF GALERİSİ
- VİDEO GALERİSİ
- e-Gazete
Gelişmelerden haberdar olmak için İstanbul Ticaret Haberleri uygulamasını indirin

Biyomedikal mühendisleri, ilaç iletimi için nanopartikülleri tasarlamada otomatik ıslak laboratuvar tekniklerini yapay zeka (YZ) ile birleştiren yeni bir platform geliştirdi. Ekip, bu yaklaşımın kapsüllenmesi zor tedavi edici ilaçların daha verimli ve etkili dağıtımına kapı açtığını bildiriyor. Kavram kanıtı çalışmasında araştırmacılar, lösemi tedavisinde kullanılan zor kapsüllenebilir bir ajanı taşıyan nanopartiküller geliştirdi ve ikinci bir kanser karşıtı nanopartikülün tasarımını optimize etti. Bulgular ACS Nano’da yayımlandı.
YAPAY ZEKA VE ROBOTİK HIZLI TASARLIYOR
Yapay zeka tabanlı araçlar, potansiyel terapötik moleküllerin biyolojik, kimyasal ve fiziksel özelliklerini öngörerek ilaç geliştirme süreçlerini dönüştürüyor. Ancak bu platformların çoğu erken aşama keşfe odaklanıyor; doğru molekül bulunsa bile, doğru yere ve doğru formda iletilmesi ayrı bir sorun olarak kalıyor. Duke ekibi, formülasyon güvenliğini ve dağıtım mekanizmalarını ileri aşamalarda optimize edebilecek bir YZ yaklaşımının eksikliğine dikkat çekiyor.
BME’de yardımcı doçent Daniel Reker’in laboratuvarında doktora öğrencisi Zilu Zhang, bir nanopartikülün performansının yalnızca “tarife”ye değil, aktif ilaç ve yardımcı maddelerin miktarlarına da bağlı olduğuna işaret ediyor. Mevcut YZ platformlarının çoğu ya malzeme seçiminde iyi ya da oran optimizasyonunda sınırlı; bu nedenle genel etkinlik kısıtlı kalıyor.
MALZEME–ORAN SARMALI
Araştırmacılar, malzeme seçim sürecini iyileştiren çeşitli makine öğrenimi modellerinin genellikle sabit oranlarla eğitildiğini, bunun da farklı oranların etkisini öğrenmeyi engellediğini vurguluyor. Reker, umut vadeden taşıyıcıların ilaçla doğru oranda karıştırılmaması halinde kararlı nanopartikül elde edilemeyeceğini belirtiyor. Daha karmaşık YZ platformları büyük veri kümelerine ihtiyaç duyarken, daha basit yaklaşımlar benzer malzemeleri ayırt etmede zorlanıyor.
YENİ PLATFORM: TUNA-AI
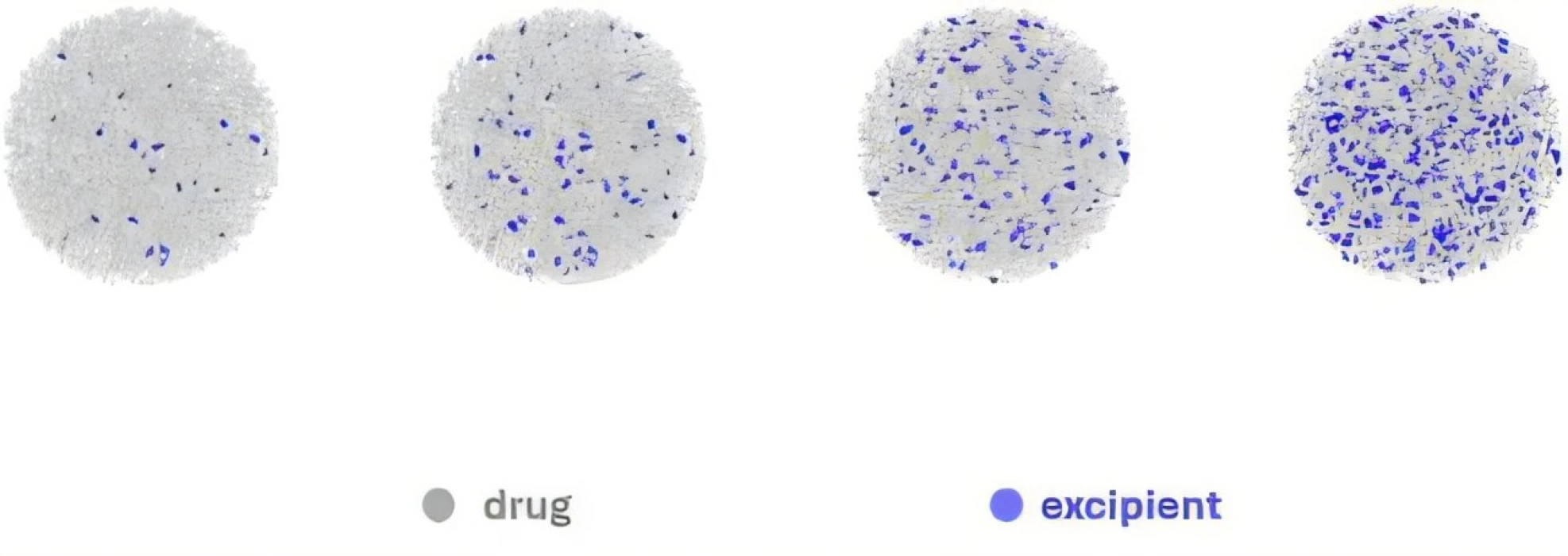
Ekip, bu darboğazı aşmak için Ayarlanabilir Nanopartikül platformu TuNa-AI’yi geliştirdi. Otomatik sıvı işleme (liquid handling) altyapısı ile 1.275 farklı formülasyondan oluşan bir veri kümesi hazırlandı. Bu veri seti; renklendiriciler, koruyucular ve ilacın fiziksel özelliklerini/amilimini iyileştiren diğer yardımcı maddeler de dahil olmak üzere çeşitli terapötik molekül–eksipiyan kombinasyonlarını kapsıyor. Zhang, robotikle çok sayıda malzemenin çok sayıda tarifte sistematik biçimde birleştirildiğini; YZ modelinin ise farklı malzemelerin farklı koşullardaki performansını öğrenerek optimum nanopartikül seçiminde kullanıldığını aktarıyor.
Sonuç olarak TuNa-AI, standart yaklaşımlara kıyasla başarılı nanopartikül oluşumunu yüzde 42,9 artırdı. Kavram kanıtında, lösemi tedavisinde kullanılan kemoterapi ilacı venetoklaks için daha etkili kapsülleme sağlandı: söz konusu venetoklaks nanopartikülleri, kapsüllenmemiş ilaca göre daha iyi çözünürlük sergiledi ve lösemi hücre proliferasyonunu daha güçlü biçimde durdurdu.
ETKİNLİK VE GÜVENLİK BİRLİKTE
İkinci bir vaka çalışmasında, yapay zeka destekli platform, ikinci bir kemoterapi ilacının formülasyonunda potansiyel olarak kanserojen bir yardımcı madde kullanımını yüzde 75 azalttı; buna karşın etkinliği korudu ve fare modellerinde biyodağılımı iyileştirdi. Zhang, TuNa-AI’nin yalnızca yeni nanoparçacıkları tanımlamakla kalmayıp, mevcut malzemeleri daha güvenli hale getirmek için de optimize edebildiğini vurguluyor.
KLİNİĞE GİDEN YOL
Ekip, platformu farklı biyomalzeme türlerini işleyebilecek şekilde genişletiyor; aynı zamanda Duke içinde ve dışında klinik araştırmacılar ile iş birliği yaparak, zor tedavi edilen hastalıklarda ilaç dağıtımını iyileştirmeyi hedefliyor. Reker, TuNa-AI’nin, terapötik uygulamalar için nanopartiküllerin tasarım ve optimizasyonunda büyük bir temel adım olduğunu, bundan sonraki aşamada mevcut ve yeni tedavileri hem daha etkili hem de daha güvenli kılmaya odaklandıklarını ifade ediyor.